Super-colture: i bioreattori
👩🏻🔬Bioreattori: la tecnologia verde che sta cambiando il volto dell'industria chimica!

Il bioreattore è l’apparecchio in cui si inducono processi microbiologici, per lo più a fini industriali o per applicazioni biomediche, tramite l’azione di microrganismi immersi nel mezzo di crescita oppure ancorati su superfici inerti fisse.
Un processo microbiologico è un processo operato da un microrganismo, indipendentemente se in condizioni di aerobiosi (presenza di ossigeno) o anaerobiosi (assenza di ossigeno), per ottenere prodotti in condizioni controllate.
In generale, un processo microbiologico è dato dalla somma di cellule e substrati per ottenere un prodotto.
I substrati devono soddisfare due aspetti principali:
- Essere in grado di rispondere alle esigenze nutrizionali dell'organismo in esame affinché esso si possa moltiplicare;
- Essere in grado di promuovere la sintesi del prodotto che si pensa di ottenere.
Il prodotto, invece, può essere rappresentato da cellule intere, metaboliti primari (prodotti essenziali per la vita e la riproduzione delle cellule) o metaboliti secondari (composti che non sono essenziali per la vita e la riproduzione delle cellule).
Classificazione dei bioreattori
I bioreattori possono essere classificati in base a tre diversi parametri:
Asetticità:
- Asettici: usati per la produzione di antibiotici, vitamine, proteine;
- Non asettici: usati in fermentazioni come la birrificazione o nel trattamento delle acque reflue.
Condizioni richieste dal bioprocesso:
- Fermentatori continuamente rimescolati o meno;
- In anaerobiosi o in aerobiosi;
- In sospensione (mezzo liquido) o su una superficie di supporto (solida).
Modalità di coltura
In questo caso è importante il metodo di somministrazione del terreno di coltura. Vediamo alcuni esempi:
- Colture in batch (a sistema chiuso): non si può avere né ingresso né fuoriuscita di materiale nel corso del processo, quindi, il volume di terreno liquido nel quale i microrganismi crescono è costante. I microrganismi, in questo caso, crescendo, riducono la quantità di nutrienti disponibile producendo metaboliti da eliminare, raggiungendo così uno stato stazionario che impedisce loro di aumentare ulteriormente di numero.
- Colture in fed-batch (sistema chiuso alimentato): si ha ingresso di substrato colturale ma non fuoriuscita di brodocoltura. In questo modo si prolunga il tempo di crescita dei microrganismi prima di raggiungere lo stato stazionario.
- Colture in perfusione: è un metodo molto usato nelle colture di cellule animali e prevede, oltre all’aggiunta di terreno fresco, anche il prelievo del terreno usato privo di cellule con i metaboliti escreti.
- Colture continue: si addiziona una certa quantità di terreno fresco e se ne sottrae una equivalente di terreno usato contenente le cellule. A differenza delle colture in perfusione, mantenendo costante la biomassa, si ottiene una crescita pressochè bilanciata in quanto anche le concentrazioni di sostanze nutrienti e di metaboliti restano essenzialmente costanti.
- Colture su strato solido: si svolgono in assenza di acqua allo stato libero e tra i substrati solidi più utilizzati si trovano legumi, cereali e altri materiali di origine vegetale.
La struttura del bioreattore
Nella maggior parte dei casi un bioreattore è costituito da un reattore di forma cilindrica ad asse verticale; tuttavia, possono essere utilizzati bioreattori ad asse orizzontale nel caso di colture algali in modo da consentire una maggiore esposizione della coltura alla luce solare o artificiale (nel caso di organismi fotosintetici).
Il volume utile per la trasformazione è di circa 2/3 del bioreattore all’interno dei quali si trova la brodocoltura (l’insieme dei microrganismi e dei prodotti), il restante 1/3 va a costituire la testata o cupola. A livello di quest’ultima vi sono una serie di entrate e di uscite provviste di valvole che hanno scopi diversi nel corso del processo.
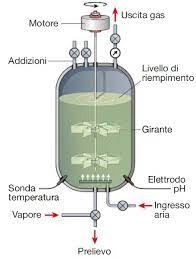
Il bioreattore presenta delle entrate utilizzate per l’aggiunta di nutriliti, sostanze nutritive necessarie per la crescita del microrganismo, o per l’aggiunta di precursori di nutriliti, di agenti per modificare il pH della brodocoltura o per controllare la formazione della schiuma che si viene a creare sulla superficie della brodocoltura.
Per quanto riguarda le uscite, una viene utilizzata per l’uscita dei gas, essa è spesso collegata a dei sistemi di refrigerazione che hanno la funzione di controllare gli effetti dovuti all’evaporazione in modo da mantenere costante il livello della brodocoltura. Inoltre, questa uscita è spesso provvista di una valvola e di un manometro che hanno la funzione di mantenere l’interno del bioreattore sterile.
Un’altra uscita si trova nella superficie inferiore del dispositivo e viene utilizzata per i prelievi di brodocoltura che vengono fatti o per controllare i vari parametri del processo (come temperatura o pH) o per scaricare tutto il bioreattore e recuperare la brodocoltura alla fine del processo.
Due caratteristiche importanti del reattore sono l’agitazione e l’aerazione.
Cosa serve ad un bioreattore con cellule in sospensione?
L'agitazione
L’agitazione ha la funzione di mantenere omogenea la brodocoltura all’interno del bioreattore evitando la sedimentazione alla base delle cellule microbiche.
Nei bioreattori che usano microrganismi aerobici l’agitazione ha la funzione di facilitare il trasporto di ossigeno la brodocoltura.
Nei bioreattori l’agitazione viene ottenuta utilizzando dei particolari dispositivi che prendono il nome di agitatori.

Essi sono costituiti da tre parti principali:
- Un motore che genera la forza rotante ed è situato nella parte superiore del bioreattore all’esterno;
- Un albero portante che entra nel bioreattore;
- Una o più giranti in cui si esplica la forza centrifuga generata dal motore.
Esistono agitatori lenti e veloci che vengono utilizzati in base alla viscosità della brodocoltura, nel caso di viscosità medio-bassa vengono usati agitatori veloci mentre per brodocolture a viscosità medio-alta vengono usati agitatori lenti.
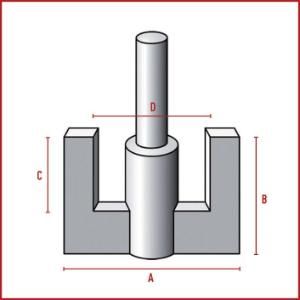
Per evitare che si vengano a formare dei vortici centrali il bioreattore è dotato anche di frangiflutti posizionati sulle pareti.
L'aerazione
Essa ha la funzione di fornire ossigeno necessario per le cellule microbiche aerobiche presenti nel bioreattore. Nel caso di cellule anaerobiche non viene fornito ossigeno ma azoto.
L’aria viene sterilizzata tramite filtri e viene poi immessa nel bioreattore tramite un dispositivo chiamato sparger, il quale, ha la funzione di suddividere l’aria in tante piccole bolle che seguono un percorso di risalita associato al movimento di agitazione per poi formare sulla superficie della brodocoltura la schiuma.
Cosa serve ad un bioreattore con cellule in adesione?
L’immobilizzazione è una procedura usata nei processi microbiologici che consiste nel confinare una cellula in superficie o all’interno di un supporto solido o semisolido per bloccarne la mobilità, senza interferire con la sua attività metabolica. Per farlo si utilizzano tecniche diverse, basate su metodi sia chimici che fisici, a seconda che si tratti di cellule o enzimi.
I bioreattori progettati per questo tipo di procedure sono di quattro tipi:
- Bioreattori di superficie: sono rappresentati dal bioreattore a tamburo, costituito da un reattore cilindrico ad asse orizzontale. All’interno è presente un tamburo ruotante la cui superficie tiene immobilizzate le cellule microbiche. Il tamburo ruotando passa periodicamente nella brodocoltura, dove le cellule immobilizzate raccolgono i nutriliti e formano il prodotto;
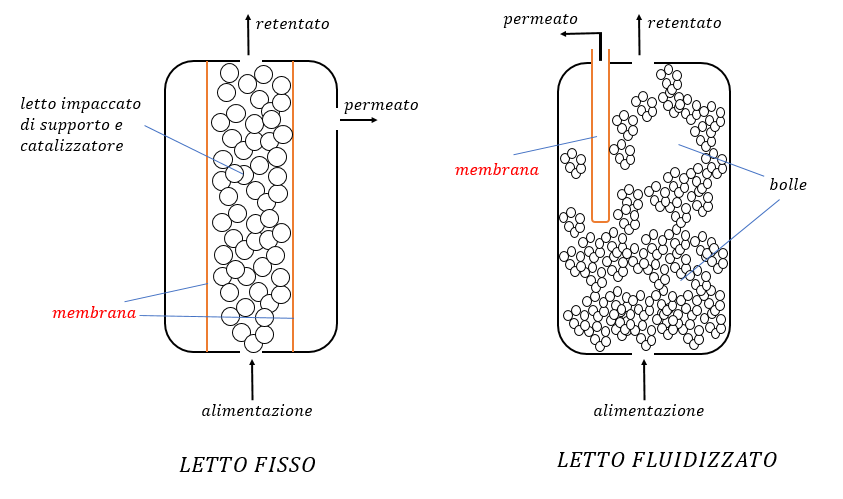
- Bioreattori a letto fisso: bioreattori cilindrici ad asse verticale che presentano all'interno dei dispositivi di ritenzione che hanno la funzione di trattenere il sistema immobilizzato in uno spazio predefinito;
- Bioreattori a letto fluido: sono cilindrici e ad asse verticale, ma non ci sono i dispositivi di ritenzione. Le cellule microbiche pur essendo intrappolate nei pori del gel non sono bloccate in uno spazio ben definito del bioreattore, ma sono in grado di muoversi in tutto il volume della brodocoltura. Il sistema immobilizzato è sospeso nella brodocoltura grazie all'equilibrio tra i flussi della fase liquida (causato da agitazione) e della fase gassosa (causata da aerazione).
- Bioreattori a membrana: dispositivo che accoppia lo svolgimento di una reazione biochimica con una separazione selettiva, che avviene tramite l'utilizzo di membrane inserite all'interno del reattore. Le membrane, invece, trattengono indistintamente tutta la biomassa e altri solidi sospesi, assicurando un effluente di alta qualità.
Esempi di utilizzi di bioreattori
- Bioreattori industriali: vengono utilizzati generalmente nel caso di batteri o altri organismi semplici in quanto hanno richieste nutrizionali semplici ed un alto tassso di riproduzione.
- Bioreattori terapeutici: hanno come obiettivo la crescita di cellule o tessuti per fini terapeutici o sperimentali. Queste cellule devono avere un supporto specifico su cui poter crescere ed inoltre ambienti continuamente mescolati possono essere deleteri per essi. Anche le richieste nutrizionali ed i fattori necessari per la crescita sono maggiori rispetto al caso precedente.
- Bioreattori ad alghe: bioreattori in grado di fornire biodiesel, metano e idrogeno molecolare.
- Dispositivi organ-on-chip: possono essere considerati dei bioreattori con integrato un sistema elettronico di controllo dei parametri, essi sono capaci di simulare in vitro organi e apparati interi.
- Piante come bioreattori: possiamo fare in modo che le colture cellulari che sono state trasformate con specifici geni funzionino come produttrici di determinate sostanze come anticorpi, vaccini edibili, proteine farmacologiche, metaboliti secondari. Un esempio è il vaccino edibile, una proteina geneticamente ingegnerizzata legata ad un antigene virale che viene codificata da un transgene nel genoma di una pianta edibile. Se ingerita, porta ad una produzione naturale di anticorpi contro quella specifica proteina vitale, la differenza dai vaccini tradizionali è che i vaccini edibili stimolano la produzione di anticorpi durante la digestione. Riguardo questo ultimo metodo sono presenti numerosi vantaggi ma altrettanti svantaggi.
Vantaggi:
- Assenza di necessità di trasporto in frigo;
- Basso costo;
- Assenza di somministrazione tramite siringhe (un minor rischio quindi di infezioni);
- Assenza di necessità di personale specializzato per la somministrazione;
- Disponibilità indefinita.
Svantaggi:
- La continuità nella produzione del vaccino è soggetta a stagionalità e cambiamenti climatici, quindi non può essere garantita;
- I vaccini edibili possono essere confusi con frutti normali ed essere consumati quindi senza controllo;
- Dosaggio variabile e difficile da controllare.
Montinaro Greta Maria
Fonti
- Appunti personali tratti dal corso di Biotecnologie dei Protisti presso il corso di laurea in Biotecnologie tenutosi dal professore Graziano di Giuseppe
- https://online.scuola.zanichelli.it/fanti2ed-files/ppt/fanti_ppt_c15_processi_biotecnologici.pdf
- https://www.treccani.it/enciclopedia/bioreattore/
- https://it.wikipedia.org/wiki/Bioreattore
- Appunti personali tratti dal corso di Biotecnologie per il miglioramento genetico presso il corso di laurea in Biotecnologie tenutosi dal professore Tommaso Giordani
- https://library.weschool.com/lezione/biotecnologie-bioreattore-crescita-cellule-terreno-temperatura-ph-sterilita-8491.html
- https://it.wikipedia.org/wiki/Reattore_a_membrana
- https://www.lenntech.it/processi/membrane-bioreactor.htm
Ti è piaciuto l'articolo?
 BioDaily.it non riceve alcun contributo pubblico né ospita alcuna pubblicità, quindi si sostiene esclusivamente grazie alle donazioni dei lettori. Ti ringraziamo qualora tu volessi fare una donazione al nostro progetto, puoi farlo cliccando su questo messaggio.
BioDaily.it non riceve alcun contributo pubblico né ospita alcuna pubblicità, quindi si sostiene esclusivamente grazie alle donazioni dei lettori. Ti ringraziamo qualora tu volessi fare una donazione al nostro progetto, puoi farlo cliccando su questo messaggio.
